最近のC型慢性肝炎のインターフェロン療法
【はじめに】
近年C型慢性肝炎の治療はdirect
acting
antivirals(DAAs)の登場により、高い治癒率を可能とする時代に入った。最も治療困難な1型高ウイルス量の症例に対して2011年に登場したDAAsの一種である第1世代プロテアーゼ阻害薬テラプレビルとペグインターフェロン、リバビリンの3剤療法は約70%の著効(SVR24)を達成したが、皮膚症状などの副作用も多く決して使いやすいものではなかった。2013年12月に第2世代プロテアーゼ阻害薬シメプレビルが発売され、これとペグインターフェロン、リバビリンの3剤療法は約90%のSVR24率で、副作用も非常に少ない素晴らしい治療法であるが、前治療無効例におけるSVR24率は50%程度にとどまっていた。2014年11月に発売された同じく第2世代プロテアーゼ阻害薬バニプレビルとペグインターフェロン、リバビリンの3剤療法も約84%の高いSVR24率であるが、特に前治療無効例において約62%とテラプレビルやシメプレビルよりよい成績を出している。
インターフェロン(IFN)を含む3剤療法の陰で、IFNが使えない患者をどう救済するのかが大きな問題であった。わが国の慢性C型肝炎患者は非常に高齢化してきており、すでに肝硬変の状態になっている人も増えてきている。IFNは高齢者には抗ウイルス効果が弱く、その特有の副作用のため治療に耐えられない人も多い。また肝硬変患者にはIFNを含む3剤療法の治療適応がないことも治療の妨げであった。
2014年9月よりNS5A増殖複合体阻害薬ダクラタスビルと第2世代プロテアーゼ阻害薬アスナプレビルによるIFNを使用しない経口薬2剤での治療が可能となり、IFNの使えない人や代償性肝硬変患者(Child-Pugh
A)にも治療の道が開かれた。2015年5月にはNS5B核酸アナログ型ポリメラーゼ阻害薬ソホスブビルとリバビリンによる2型のC型慢性肝炎に対する経口2剤治療が、そして2015年秋にはソホスブビルとNS5A増殖複合体阻害薬レディパスビルによる1型に対する経口2剤治療が可能になる予定であり、治療の可能性は大きく広がり続けている。高い治癒率が期待でき目立った副作用もなく、高齢者や代償性肝硬変患者も含めた広い治療適応があると思われるが、耐性ウイルスについての十分な注意が必要である。これら経口薬のみによる治療については別章にて詳述されているので、そちらを参照されたい。
「C型慢性肝炎治療ガイドライン」として、厚生労働省研究会編のものと日本肝臓学会編のものがあり、実際の治療にあたっては、この両者を熟読する必要があることは言うまでもないが、新規治療薬が早いペースで登場するのに合わせて、ガイドラインも短期間で改訂が繰り返され、記載の分量もかなり大きなものとなっている。本章ではガイドラインの内容すべてを網羅することはせず、図表を多用し筆者の私見も交えて肝臓病非専門の先生にもミニマムエッセンシャルな内容を理解しやすく伝えることに注力することにした。
【診断から治療までの流れ】
まずはHCV抗体の測定がスタートとなる。ここで強調したいことは、「慢性肝炎」という言葉につられてALT値が異常値の患者のみに意識を向けがちであるが、フローチャートを見るとわかるようにALT値はフローチャートのスタートではないことである。ALT持続正常者(PNALT)の中にもC型肝炎ウイルス(HCV)感染者は存在するし、これらの患者は年数の経過とともにALT値の上昇や肝臓の線維化が進行することがわかっているので、場合によっては治療の対象となりうる。自治体による「ウイルス肝炎検診」制度などを活用し、可能な限り多くの人にHCV抗体検査を行って治療対象者の掘り起しの努力を行うことが必要である。
HCV抗体陽性者に次に行う検査はHCV-RNAの測定である。可能な限り測定感度の高い検査方法で行うべきである。「検出なし」の場合は、HCVの感染既往の状態で、HCVに感染した後に自然にウイルスが排除されたり、過去に受けたIFN治療などによりウイルスが排除されたりしている状態である。たとえウイルスが排除されていてもHCV抗体は感染の既往として陽性のままであることに注意されたい。HCV-RNA「検出なし」の場合ここで治療の対象からは外れることになる。
HCV-RNAが検出され、ALT値が30を超えている場合はすでに治療開始すべき状態と考えられる。30以下の場合は2~4月ごとに採血フォローアップを行い、肝臓の線維化進行を反映している血小板数が15万をきるか、肝臓の炎症を反映しているALT値が30を超えるかすれば、治療開始を考慮する。
この時点で、治療方法の選択のためHCV群別により1型か2型かを調べ、HCV-RNAの定量結果とあわせて、治療方法の検討に入ることになる。
【肝硬変を見落とさないために】
IFNを含む3剤療法(ペグリバ24シメプレ12またはペグリバ24バニプレ12)は肝硬変に対する適応がないため、肝硬変でないことを確認する必要がある。血小板数が10万をきっている症例では肝硬変となっている可能性がある。IFNを使用しない経口2剤療法(ダクラアスナ24またはソホリバ12など)は代償性肝硬変(Child-Pugh
A)に対する適応があるが、治療中に出現するかもしれない副作用による肝障害には格別の注意を払う必要がある。
Child-Pugh分類の表を参考までに掲載した。
【インターフェロン】
インターフェロン(IFN)は人間等がウイルス感染を受けた時などに体の中で作られるタンパク質の一種であり、主な作用として抗ウイルス作用、免疫増強作用、抗腫瘍作用などがある。IFN-αとβは(T細胞、B細胞)リンパ球、マクロファージ、線維芽細胞、血管内皮細胞、骨芽細胞など多くのタイプの細胞で産生され特に抗ウイルス応答の重要な要素である。
C型慢性肝炎治療に認可されているIFNはα型とβ型がある。α型ではポリエチレングリコール(PEG)がIFNに結合しているか否かによって、非PEG化製剤(天然型IFNαと遺伝子組み換えIFNα-2b)とPEG化製剤(PegIFNα-2aとPegIFNα-2b)がある。β型は天然型IFNβで非PEG化製剤である。
非PEG化製剤は不安定で血中半減期は短く、慢性肝炎治療においては少なくとも週3回の注射を必要とする。また、血中濃度の上昇・下降を繰り返すため発熱・悪寒・頭痛などの副作用を伴いやすい。一方PEG化製剤は安定して長く血中濃度が維持されるため、週1回の注射ですみ副作用も軽減されている。2種類のPEG化製剤は標準投与量が異なっているため注意すること。現時点において2種類のPEG化製剤は有効性・副作用の点でほぼ同等と考えられる。
IFNβは天然型で静注または点滴静注で週3回以上の投与を行う。PegIFNα併用治療に比し、血小板の低下やうつなどの副作用が少ないため、うつなどでIFNαが投与できない症例では、天然型IFNβを用いる治療選択肢がある。
IFN使用時は大なり小なり副作用はほぼ必発である。なかでも全身倦怠感・食欲低下・発熱・頭痛・関節痛などのインフルエンザ様症状は最もよくみられ、60~95%の患者に認められる。白血球・好中球・血小板の減少は投与開始4週までに進行し、その後定常状態になることが多い。抑うつ・不眠などの精神症状も5~10%に認められ、うつの既往や治療前精神症状がある症例で起こりやすい。慢性甲状腺炎などの自己免疫性疾患を惹起または増悪させる可能性がある。間質性肺炎は治療開始2ヶ月以降や治療後期に起こることが多い。注射部位や全身の発疹・かゆみなどの皮膚症状、脱毛、糖尿病、心筋症や網膜症・眼底出血も副作用として起こりうる。
IFNによってC型肝炎ウイルス(HCV)が排除された場合はもちろん、排除されなかった場合においても、治療後の肝細胞癌の発癌リスクは低下することが多く報告されている。
【リバビリン】
リバビリン(ribavirin)は、免疫誘導作用・ウイルスの変異誘導・RNAポリメラーゼの抑制・細胞内GTPの枯渇作用などにより抗ウイルス活性を示す。リバビリンの単独投与ではC型慢性肝炎への治療効果は乏しいがIFNとの併用により優れた効果を示す。1日2回、朝・夕食後に経口投与する。リバビリンには体内に蓄積性があり、排泄は主に腎臓で行われるため腎機能低下例には慎重に投与する必要がある。クレアチニンクリアランス50ml/min以下では禁忌である。透析では除去不能のため、透析中の患者に投与してはならない。
主な副作用は溶血性貧血で、貧血や心疾患を有する患者への適応は慎重を要する。投与開始前Hb14g/dl未満、好中球2000/μlあるいは血小板数12万/μl未満、および女性や高齢者では薬剤の減量を要することが多い。投与中にHb低下がみられた場合Hb10未満で200mg減量、8.5未満で中止である。ただし減量・休薬によりSVR率は低下するので、貧血を適切に管理して可能な限り投与を完遂させるよう努めることが重要である。PegIFN+リバビリン併用療法に伴う高度貧血に、患者のinosinetriphosphatase(ITPA)遺伝子多型が関与している。CCゲノタイプ(major
homo)では治療中の貧血の進行に注意すること。貧血以外にリンパ球減少・高尿酸血症・掻痒感・皮疹・咳嗽・鼻閉などの副作用がある。
催奇形性の報告があり、妊娠中または妊娠の可能性のある女性、授乳中の女性への投与は禁忌。妊娠する可能性のある女性、パートナーが妊娠する可能性のある男性には避妊を指示すること。
【Direct
Acting Antivirals (DAAs)】
現代におけるC型慢性肝炎治療はDAAsなしには考えられない。よって、今後登場するものを含めて、多くのDAAsの特徴について十分に知ることが重要である。
(1)テラプレビル(telaprevir)
第1世代NS3/4Aプロテアーゼ阻害薬であり1型HCVに対するウイルス増殖抑制作用が強い。2011年9月にPegIFNとリバビリンとの3剤併用(ペグリバ24テラプレ12)として1型高ウイルス量に対して、また2014年9月に2型でIFN(+リバビリン)による前治療再燃・無効例に対しても適応追加となった。
副作用としては皮膚症状・貧血・腎障害・高尿酸血症などがあり、とくに重篤な皮膚症状を生じうるため治療にあたっては皮膚科医との連携の上行うことが必要である。貧血の進行についてはHb値を定期的に測定し、リバビリンの減量により対処する。投与開始初期にクレアチニン上昇・尿酸の上昇をみることがある。65歳以上の患者では副作用の予防のため減量投与が必要な可能性がある。なお肝硬変患者への適応はない。
薬物代謝酵素CYP3A4/5を強力に阻害するため、多くの薬剤が併用禁忌・併用注意となっている。
テラプレビルによる治療が失敗した場合に生じるウイルスの耐性変異はV36,T54,R155,A156,V170があるが、治療終了後時間の経過とともに耐性ウイルスはなくなっていくと考えられている。
(2)シメプレビル(simeprevir)
第2世代NS3/4Aプロテアーゼ阻害薬であり1型HCVに対するウイルス増殖抑制作用が強い。2013年9月にPegIFNとリバビリンとの3剤併用(ペグリバ24シメプレ12)として1型高ウイルス量に対して適応となった。
副作用としては肝トランスポーター活性の阻害による一過性の軽度のビリルビン上昇がみられることがある程度で、重篤な皮膚症状はみられない。その他の副作用もPegIFN+リバビリン2剤併用療法と同等程度で治療完遂率は高い。なお肝硬変患者への適応はない。
主にCYP3Aにより代謝され、OATP1B1とP糖蛋白質を阻害するため併用禁忌・併用注意薬を確認すること。
シメプレビルによる治療が失敗した場合に生じるウイルスの耐性変異はD168であるが、治療終了後時間の経過とともに耐性ウイルスはなくなっていくと考えられている。
(3)アスナプレビル(asunaprevir)
シメプレビルと同様の第2世代NS3/4Aプロテアーゼ阻害薬であり1型HCVに対するウイルス増殖抑制作用が強い。2014年7月にIFNを含む治療法に不適格・不耐容の患者ならびにIFNを含む治療法で無効となった患者に対して、制限つきで後述のダクラタスビルとの経口2剤療法(ダクラアスナ24)として保険認可となった。そして2015年3月より制限が撤廃され、1型慢性肝炎と代償性肝硬変(Child-Pugh
A)すべてに保険認可された。
経口2剤療法については別章にて詳述されているので、そちらを参照されたい。
(4)ダクラタスビル(daclatasvir)
初めて開発され臨床応用されたNS5A阻害薬であり、さまざまな型のHCV増殖抑制に強力な作用を示す。前述のアスナプレビルとの経口2剤(ダクラアスナ24)として2014年7月、2015年3月保険認可された。
(5)バニプレビル(vaniprevir)
シメプレビルやアスナプレビルと同様の第2世代NS3/4Aプロテアーゼ阻害薬であり1型HCVに対するウイルス増殖抑制作用が強い。2014年11月にPegIFNα2bとリバビリンとの3剤併用(ペグリバ24バニプレ12)として1型高ウイルス量に対して適応となった。ただしIFNを含む前治療で無効となった症例(non-responder)に対してはバニプレビルを24週投与する(ペグリバ24バニプレ24)点がシメプレビル3剤療法と異なる。
副作用としては軽度から中等度の胃腸障害(嘔吐、悪心、下痢)が投与初期にみられることが多い。なお肝硬変患者への適応はない。
主にCYP3Aにより代謝され、OATP1B1とP糖蛋白質を阻害するため併用禁忌・併用注意薬を確認すること。
バニプレビルによる治療が失敗した場合に生じるウイルスの耐性変異はR155,A156,D168である。
(6)ソホスブビル(sofosbuvir)
初めて開発され臨床応用された唯一のNS5B阻害薬であり、さまざまな型のHCV増殖抑制に強力な作用を示す。2015年5月ごろ、2型の慢性肝炎および代償性肝硬変(Child-Pugh
A)に対し、リバビリンと併用での経口2剤療法(ソホリバ12)として保険認可の予定である。
【インターフェロンとDAAsの特徴について】
インターフェロン(IFN)は人間の免疫系に働きかけ、非特異的にウイルス排除に作用する一方、DAAsはウイルスそのものに働きかけ、ウイルスの増殖を特異的にブロックする。IFNが人間の体への作用を主としているため、その裏返しとしての多彩な副作用が避けられない。DAAsはウイルスへの直接作用であるため、うまくいけば人体への副作用が極めて少なくてすむことが期待される。実際の治療にあたっては、IFN治療の場合、投与される人間側(ホスト側)の要因が効果や副作用に影響を与えることが多く、DAAs治療の場合、ホスト側の要因はほとんど無関係であり、DAAsに対するウイルスの耐性の有無が治療効果を左右するのである。
IFN治療に影響を与えるホスト側の要因としては、性別(男性の方が効きやすい)、年齢(高齢者ほど効きにくい)、肝臓の線維化(線維化進展例ほど効きにくい)、IL28Bの遺伝子多型(TTが効きやすくTG/GGは効きにくい)、ITPA遺伝子多型(CCゲノタイプ
は貧血になりやすい)などがあり、ウイルス側の要因としてはISDR: interferon
sensitivity determining region
(wild効きにくい)、Core70(mutant効きにくい)などがある。
DAAs治療に影響を与えるウイルス側の要因としては、HCVの耐性変異の存在である。治療前からある程度の割合で耐性変異が存在しており、また耐性がない場合でも治療中に耐性変異が出現する場合もある。耐性ウイルスが存在あるいは出現した場合、DAAsによる治療が失敗し、DAAsに対する多剤耐性ウイルスが長期に残存し、その後の治療が困難になる恐れがある。したがって、DAAsの治療に先立って、使用しようとするDAAに対するHCVの耐性変異が存在しないかどうかを確認しておくことは重要である。ダクラアスナ24を行う前には、アスナプレビル耐性となるD168、ダクラタスビル耐性となるL31,Y93のチェックは必ず行うようにしたい。耐性の存在により経口剤による治療の失敗の恐れがある場合、経口2剤ではなくIFNを含む3剤療法を検討する余地があると思われる。IFNは先に述べた特質により、DAAsの薬剤耐性とは関係なく効果を発揮するし、治療中に出現するかもしれない耐性ウイルスを排除する効果が期待しうるからである。
IFNを使用した治療によりSVRとなり、ウイルス排除できた症例については、その後の肝発癌リスクが低下することが多く報告されている。一方IFNを使用しない経口剤のみによってウイルス排除できた症例について同様に肝発癌リスクが低下するかどうかについては、長期にわたる観察ができていないため不明である。
参考までに、IFNを含む治療と経口2剤による治療についてメリットとデメリットを簡単に表でまとめてみた。
【治療の選択にあたって】
前項で述べたIFNとDAAsの特徴を頭に入れた上で、実際の治療の選択にあたっての考え方を私見も交えて示す。
HCV1型で、IFN治療が不適格の未治療例や前回のIFN治療に耐えられなかった症例では、IFNを使用しない経口2剤療法(現在ではダクラアスナ24)を選択する。
HCV1型で、IFN治療が適格の高ウイルス量(5Log以上)の初回治療例あるいは前回の治療後に再燃した症例では、IFN治療の受け入れが可能であれば、IFNを含む3剤併用療法(ペグリバ24シメプレ12またはペグリバ24バニプレ12)を選択する。2015年3月より経口2剤(ダクラアスナ24)の制限が撤廃されたために、IFN治療の受け入れが不可(IFN投与を受けたくないなど)の場合、経口2剤の選択も可能である。この場合事前にNS5A/NS3耐性の検討を必ず行うべきである。
HCV1型で、IFN治療が適格の低ウイルス量(5Log未満)の初回治療例では、IFN単独24週間あるいはPeg-IFNα2a単独24~48週間投与を行う。ただしIFNの受け入れが不可の場合は、NS5A/NS3耐性の検討の上で経口2剤(現在ではダクラアスナ24)を行う。
IFNを含む前の治療に対して無効だった(治療中ウイルスの消失がなかった)症例(non
responder)に対しては、NS5A/NS3耐性検査を行い耐性変異がなければ、経口2剤療法(現在ではダクラアスナ24)を選択する。残念ながら、耐性変異を認める場合は、IFNの受け入れが可能で、シメプレビルやバニプレビル耐性となるD168の変異がなければペグリバ24シメプレ12あるいはペグリバ24バニプレ24を選択することも可能である。D168の変異がある場合は前治療から24週以上待機してD168の変異が消えるのを待って治療に入るか、次世代の経口2剤療法(レディパスビル+ソホスブビル)を待つのもよいかもしれない。
最も困難なnon
responderでNS5A/NS3耐性もあり、IFNの受け入れ不可の症例の場合は、無理をして経口2剤(ダクラアスナ24)を行って失敗し多剤耐性となるよりも、待機が可能であれば次世代の経口2剤療法(レディパスビル+ソホスブビル)を待つのもよいかもしれない。ただし待機するにあたっては、肝発癌リスクを十分考慮した上で決定すべきである。
HCV2型に対する初回治療はウイルス量により2つに分かれる。高ウイルス量(5Log以上)では、Peg-IFN(またはIFNβ)とリバビリンの2剤併用24週間投与を行う。IFN投与に伴う、うつなどの副作用が予想される症例や、高齢者で副作用出現が予測される症例ではIFNβを選択する。低ウイルス量(5Log未満)ではIFN単独8~24週あるいはPeg-IFNα2a単独24~48週投与を行う。IFN単独療法で2週以内にHCV-RNAが陰性化する症例では8~16週に短縮することも可能である。
HCV2型に対する再治療はウイルス量にかかわらず、Peg-IFNα2bとリバビリン24週+テラプレビル12週で行う。テラプレビルの投与量は1500mgを基本とし適宜増減する。HCV2型においても2015年5月ごろに、ソホスブビルとリバビリン12週間(ソホリバ12)の経口2剤療法が保険認可される予定である。おそらくはIFN不適・不耐容症例であるなしにかかわらず、HCV2型においてはソホリバ12による治療が主流となるのではないかと考えている。
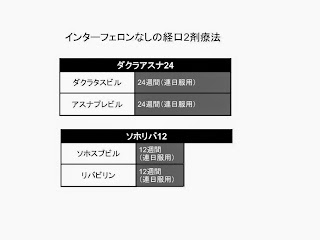
【治療レジメン】
いままでに説明した各治療レジメンについて、簡単に以下に図示した。実際の投与量については患者の体重や貧血の状態などにより変わってくるため、薬剤の添付書を熟読する必要がある。IFNを含む治療は肝硬変に対しては適応がないことに注意すること。バニプレビルを使用するレジメンでは、1型Non
responderに対してはバニプレビル24週投与を行う。
|
|
|
|
|
血小板数が5万以下の肝硬変症例では、IFNの治療効果を十分検討の上、脾臓摘出手術あるいは脾動脈塞栓術を施行して血小板数の増加をはかり、その後IFN(リバビリン併用も含む)治療を行うことが可能である。
IFNを含まない経口2剤療法は慢性肝炎に対するのみならず代償性肝硬変(Child-Pugh
A)に対する適応がある。治療の前にはNS5A/NS3耐性の有無について検討しておくことが重要である。
経口2剤療法については別章にて詳述されているので、そちらを参照されたい。
|
【進展予防(発がん予防)の治療】
プロテアーゼ阻害薬(テラプレ、シメプレ、バニプレ)を含む3剤併用療法およびリバビリン併用療法の非適応例、あるいはリバビリン併用療法で無反応例の中で発がんリスクの高い症例(50歳以上F2以上)では、IFNの副作用の素因を考慮し、発がん予防目的のIFN長期投与が選択肢となる。IFNα製剤は300万単位/日を3回/週を原則とし、PEG製剤を除いて在宅自己注射も可能である。Peg-IFNα2a製剤を使用する場合は90μg/日を1~2週間に1回使用する。
IFN非適応例およびIFNでALT値・AFP値の改善がない症例では、肝庇護剤(SNMC:強力ネオミノファーゲンC、UDCA:ウルソデオキシコール酸)の投与や瀉血療法を単独あるいは組み合わせて治療する。
進展予防(発がん予防)の治療でのALTの目標値は、F1では持続的に基準値上限の1.5倍以下に、F2~F3ではALT30以下にコントロールする。
【治療中止基準】
Peg-IFNα+リバビリン+プロテアーゼ阻害薬を含む3剤併用療法の場合、治療開始後12週後にHCV-RNAが陰性化しない症例は治療を中止する。また、治療期間中にbreakthrough(2回連続してHCV-RNAの最低値から2Logを超えて増加)した場合も治療を中止する。
Peg-IFNαまたはIFNβ+リバビリン2剤併用療法の場合、治療開始後12週後にHCV-RNAが開始時に比し2Log以上の低下がなく、HCV-RNA陽性のままで36週まで陰性化なく、かつALT・AST値が正常化しない症例は36週の時点で治癒目的の治療は中止する。しかし、治療開始後12週後にHCV-RNAが開始時に比し2Log以上の低下がみられ、ALT値が正常化した症例は48週まで継続投与を行い、治療終了後の長期ALT値正常化維持を期待する。
IFN単独投与の場合、治療開始6ヶ月以内にALT値(40以下)あるいはAFP値(10以下)の有意な改善がみられない場合は、発がん予防効果が期待できないため治療を中止する。
【ウイルス学的反応の定義】
ウイルス学的反応
|
定義
|
Rapid
virological response (RVR)
|
治療開始後4週でHCV-RNA感度以下
|
Extended
RVR
|
治療開始後4週・12週いずれもHCV-RNA感度以下
|
Early
virological response (EVR)
|
cEVRあるいはpEVR
|
| Complete EVR (cEVR) |
治療開始後12週でHCV-RNA感度以下
|
| Partial EVR (pEVR) |
治療開始後12週でHCV-RNAが2Log以上低下するも陽性のまま
|
End-of-treatment
response (ETR)
|
治療終了時HCV-RNA感度以下
|
Sustained
virological response 24 (SVR24)
|
治療終了後24週の時点でもHCV-RNA感度以下
|
Breakthrough
|
治療中いったん感度以下となったHCV-RNAが治療中に再度陽性に
|
Relapse
|
治療中いったん感度以下となったHCV-RNAが治療終了後に再度陽性に
|
Non
responder
|
治療中にHCV-RNA感度以下にならず(Null
and Partial responder)
|
| Null responder |
治療開始後12週でHCV-RNAが2Log以上低下せず、陽性のまま
|
| Partial responder |
治療開始後12週でHCV-RNAが2Log以上低下するが、しかし24週でも陽性のまま
|
【参考】
・平成27年B型C型慢性肝炎・肝硬変治療のガイドライン(厚生労働省 肝炎等克服緊急対策研究事業)
・C型肝炎治療ガイドライン 第3.3版 (日本肝臓学会 肝炎治療ガイドライン作成委員会)
・内科処方実践マニュアル 改訂第2版 (日本臨床内科医会)
・これだけは知っておきたいC型肝炎・B型肝炎の知識 平成25年度改訂版
(神奈川県内科医学会 肝炎対策委員会)









0 件のコメント:
コメントを投稿